筋萎縮性側索硬化症で、加齢により運動野の細胞が侵される謎に迫りました
2021年09月27日
本研究所脳神経内科・分子神経疾患資源解析学分野の 小池 佑佳 博士研究員 (米国・メイヨークリニック留学中)、須貝 章弘 助教、小野寺 理 教授らの研究グループは、同研究所病理学分野 柿田 明美 教授ら、遺伝子機能解析学分野 池内 健 教授らとの共同研究により、筋萎縮性側索硬化症 (amyotrophic lateral sclerosis: ALS) の発症機序に、「DNAのメチル化」が関わっていることを明らかにしました。本研究により、「TDP-43の量の自己調節」に関わるDNA領域は、運動野(※1)で、加齢に伴い、脱メチル化し、TDP-43の量の増加につながることがわかりました。本研究成果は、「Communications Biology」誌に、2021年9月21日に公開されました。
研究成果のポイント
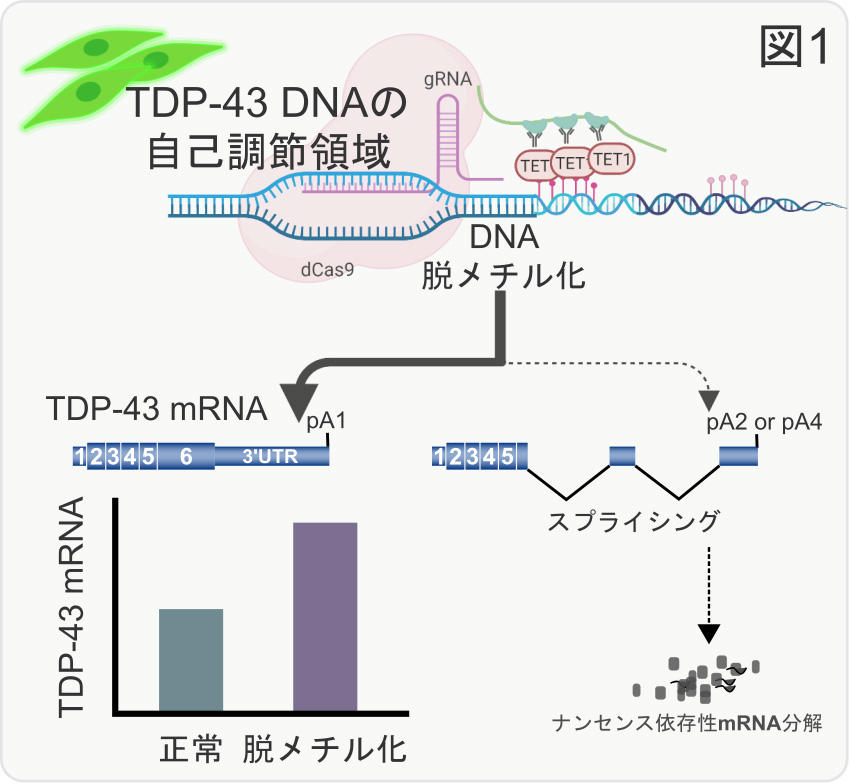
- ALSの原因となるタンパク質 (TDP-43)の量の自己調節機構に関わるDNA領域のメチル化が失われると(脱メチル化)、TDP-43遺伝子の発現が増加することを示しました (図1, 図2)。
- 正常者では、ALSで侵される運動野で、加齢によって、この部位の脱メチル化が進み、TDP-43遺伝子の発現が増加することを明らかにしました (図2)。
- ALS患者さんでは、この部位が脱メチル化されている程、病気になる年齢が若くなることを明らかにしました (図3)。
Ⅰ.研究の背景
ALSは中年期以降に発症し、運動野の神経細胞を障害する難病です。この、特定の場所を、加齢により侵すという特徴は、ALSの最大の謎であり、ここに、本症解明の鍵があると考えられています。
本症では、TDP-43 (Transactivation responsive region DNA-binding protein of 43kDa) というタンパク質が、細胞の中に溜まります。TDP-43の量が増えると溜まりやすくなり、細胞に障害を引き起こします。そのため、正常な細胞では、TDP-43の量が増え過ぎないように厳密に調整されています。
TDP-43タンパク質が過剰な場合は、TDP-43自身のメッセンジャーRNA (mRNA) (※2)に作用して、スプライシング(※3)という仕組みを使って、このmRNAを破壊して、TDP-43タンパク質の量を減らします。これは、「TDP-43の量の自己調節」と呼ばれる機構です。これまでに本研究グループでは、この機構の仕組みを明らかにしてきました。しかし、TDP-43の量の自己調節機構がありながら、何故、年をとると運動野の細胞にTDP-43が溜まりやすくなるのかは、明らかになっていませんでした。
Ⅱ.研究の概要・成果
 年をとると、DNAにさまざまな変化がおきます。その一つに「DNAのメチル化」があります。これは、タンパク質の設計図であるDNAの一部にメチル基 (CH3)が加わることを指します。DNAの様々な部位が、メチル化されます。このメチル化の程度が変わることで、同じDNAでありながら、作られるタンパク質の量や種類が変わります。同じDNAから、様々な臓器ができる仕組み、親の経験が子に伝わる仕組み、レット症候群などの病気の背景になっています。遺伝子、身体の部位毎に、DNAのメチル化の程度は異なります。
年をとると、DNAにさまざまな変化がおきます。その一つに「DNAのメチル化」があります。これは、タンパク質の設計図であるDNAの一部にメチル基 (CH3)が加わることを指します。DNAの様々な部位が、メチル化されます。このメチル化の程度が変わることで、同じDNAでありながら、作られるタンパク質の量や種類が変わります。同じDNAから、様々な臓器ができる仕組み、親の経験が子に伝わる仕組み、レット症候群などの病気の背景になっています。遺伝子、身体の部位毎に、DNAのメチル化の程度は異なります。
DNAのメチル化の程度は、脳部位によっても異なり、加齢の影響を受けます。また、ALSを発症する最大の危険因子は加齢です。これらから、本研究では「TDP-43の量の自己調節」に関与するDNA領域のメチル化に着目しました。
まず細胞で、「TDP-43の量の自己調節」に関与するDNA領域を選択的に脱メチル化させました。その結果、この領域の脱メチル化は、TDP-43自身のmRNAのスプライシングを阻害し、TDP-43遺伝子の発現量を増加させることを明らかにしました (図1)。すなわち、この特定のDNA領域のメチル化が、TDP-43の量の自己調節機構に影響を及ぼしていることを示しました。
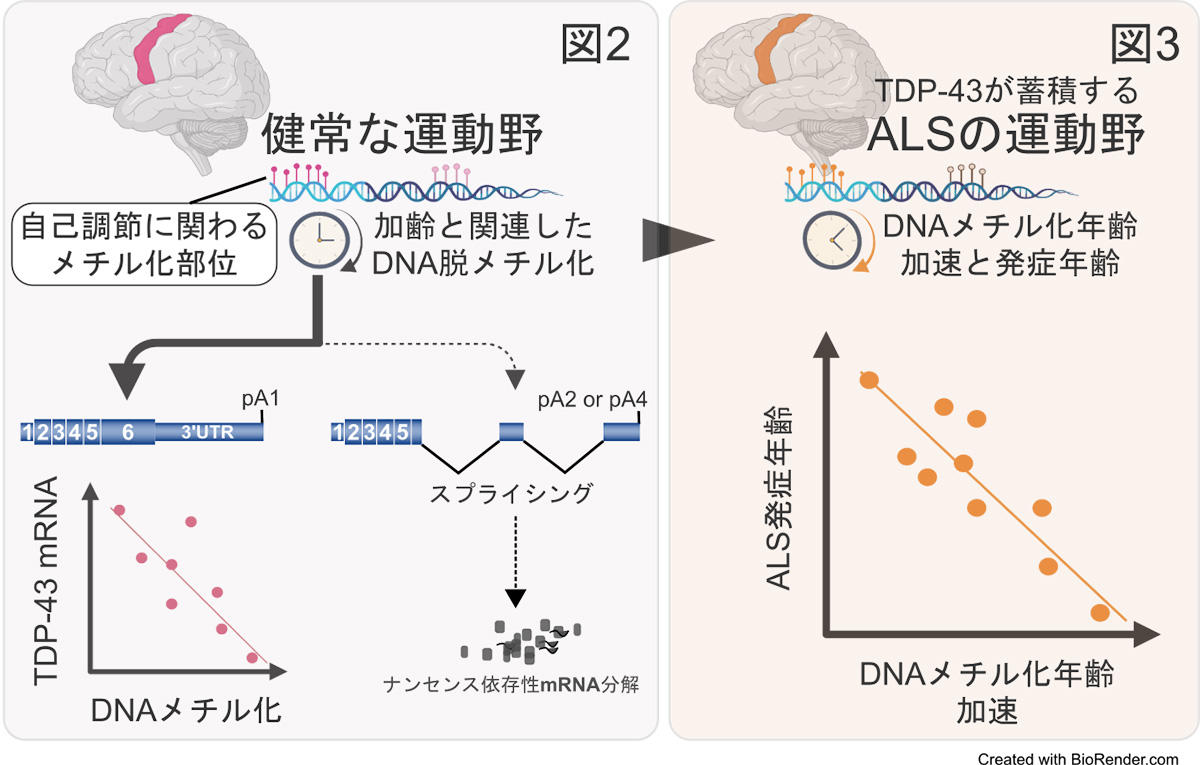 次にヒトの脳組織で、「TDP-43の量の自己調節」に関与するDNA領域のメチル化状態を調べました。その結果、このDNA領域のメチル化状態は、脳の部位によって、異なっていることが分かりました。興味深いことに、疾患がなかった健常な脳の運動野では、このDNA領域は加齢とともに脱メチル化することが明らかになりました。さらに、細胞の実験結果から予想されたように、「TDP-43の量の自己調節」に影響する脱メチル化と、TDP-43遺伝子の発現量の増加には、相関関係があることが確認されました (図2)。TDP-43は、量が増えると細胞に溜まりやすくなり、細胞に障害を引き起こします。そこで、運動野のTDP-43タンパク質の量を調べると、このDNA領域の脱メチル化が進むほど、TDP-43が溜まっていました。これらの結果は、ALSにおいて、加齢により運動野の細胞が侵される謎には、「TDP-43の量の自己調節」に影響するDNAのメチル化が関わっている可能性を示しました。
次にヒトの脳組織で、「TDP-43の量の自己調節」に関与するDNA領域のメチル化状態を調べました。その結果、このDNA領域のメチル化状態は、脳の部位によって、異なっていることが分かりました。興味深いことに、疾患がなかった健常な脳の運動野では、このDNA領域は加齢とともに脱メチル化することが明らかになりました。さらに、細胞の実験結果から予想されたように、「TDP-43の量の自己調節」に影響する脱メチル化と、TDP-43遺伝子の発現量の増加には、相関関係があることが確認されました (図2)。TDP-43は、量が増えると細胞に溜まりやすくなり、細胞に障害を引き起こします。そこで、運動野のTDP-43タンパク質の量を調べると、このDNA領域の脱メチル化が進むほど、TDP-43が溜まっていました。これらの結果は、ALSにおいて、加齢により運動野の細胞が侵される謎には、「TDP-43の量の自己調節」に影響するDNAのメチル化が関わっている可能性を示しました。
DNAのメチル化の程度から、私達の身体の本当の年齢(生物学的な年齢)を推定できます。生物学的な年齢は、さまざまな疾患の発症に関係していることが知られています。そこで、「TDP-43の量の自己調節」に影響するDNA領域の脱メチル化の程度から、ALS患者さんの運動野における生物学的な年齢を推定しました。その結果、生物学的な年齢が進んでいる程、ALSを発症する年齢が若くなることが示されました (。すなわち、「TDP-43の量の自己調節」のDNA領域の脱メチル化は、ALSを発症する年齢と関連することが分かりました。
Ⅲ.今後の展開
本研究により、TDP-43の量の自己調節に関わるDNA領域は、運動野で加齢に伴い脱メチル化し、TDP-43の量の増加につながることがわかりました。これにより、今まで謎であった、加齢により、特定の場所に病気が引き起こされる謎の手がかりがつかめました。さらに、ALSの患者さんでは、この現象がALSの発症と関連する可能性があります。したがって、TDP-43の量の自己調節に関わるDNA領域のメチル化状態は、ALSに対する有望な治療標的になる可能性があります。
Ⅳ.研究成果の公表
この研究成果は、Nature Researchが提供するオープンアクセス・ジャーナルで、生物科学の全分野における高品質な論文・総説・論評を出版している「Communications Biology」誌(IF=6.27)に、2021年9月21日 (英国時間) に公開されました。
| 【論文タイトル】 |
Age-related demethylation of the TDP-43 autoregulatory region in the human motor cortex |
| 【著者】 |
Yuka Koike, Akihiro Sugai, Norikazu Hara, Junko Ito, Akio Yokoseki, Tomohiko Ishihara, Takuma Yamagishi, Shintaro Tsuboguchi, Mari Tada, Takeshi Ikeuchi, Akiyoshi Kakita, Osamu Onodera |
| 【doi】 | 10.1038/s42003-021-02621-0 |
Ⅴ.本研究への支援
本研究は、文部科学省科学研究費補助金 新学術領域研究「脳タンパク質老化と認知症制御」、日本学術振興会 科学研究費助成事業 基盤研究 (A)、基盤研究 (C)、研究活動スタート支援、厚生労働科学研究費補助金 難治性疾患政策研究事業、武田科学振興財団、椿神経疾患研究基金、せりか基金からの支援により、実施しました。
【用語解説】
※1運動野:
骨格筋に運動の指令を出す、脳の領域を指します。ALSでは、この領域に存在する神経細胞が、選択的に障害を受けることが知られています。
※2メッセンジャーRNA (mRNA):
遺伝子からタンパク質が合成される過程では、まず、DNAを鋳型にして、メッセンジャーRNA (mRNA) が作られます。その次に、このmRNAからタンパク質が作られます。
※3 スプライシング:
mRNAのうち、タンパク質の合成に関わる部分のみを残し、タンパク質の合成に関わらない部分は取り除く仕組みです。これにより、一つの遺伝子から複数のmRNAを産生することが可能となり、限られた遺伝子情報から、多様性のあるタンパク質を合成することができます。また、スプライシングのされ方によって、分解されやすいmRNAが生じることがあり、これにより、タンパク質の発現量を調整している遺伝子があります。





