ひと剖検脳の三次元イメージングにより脳アミロイド血管症における血管アミロイド沈着の空間的分布を解明
2026年02月10日
概要
新潟大学医歯学総合病院脳神経内科の林秀樹助教、同大学脳研究所脳疾患標本資源解析学分野の齋藤理恵助教、同研究所病理学分野の柿田明美教授らの研究グループは、同研究所システム脳病態学分野の田井中一貴教授と共同で、脳アミロイド血管症(CAA)患者脳におけるアミロイドβ(Aβ)沈着の三次元的進展様式を明らかにし、その成果を米国科学雑誌 Science Advances に発表しました。
本研究では、CAA患者剖検脳に高度組織透明化技術と光シート顕微鏡を組み合わせた三次元(3D)イメージング解析を適用し、Aβ沈着が脳表動脈から深部血管へと解剖学的に連続して進展することを、ひとの脳で実証しました。この知見は、CAAおよびアルツハイマー病関連血管病変の病態理解を深め、新たな治療標的の検討につながることが期待されます。
本研究成果のポイント
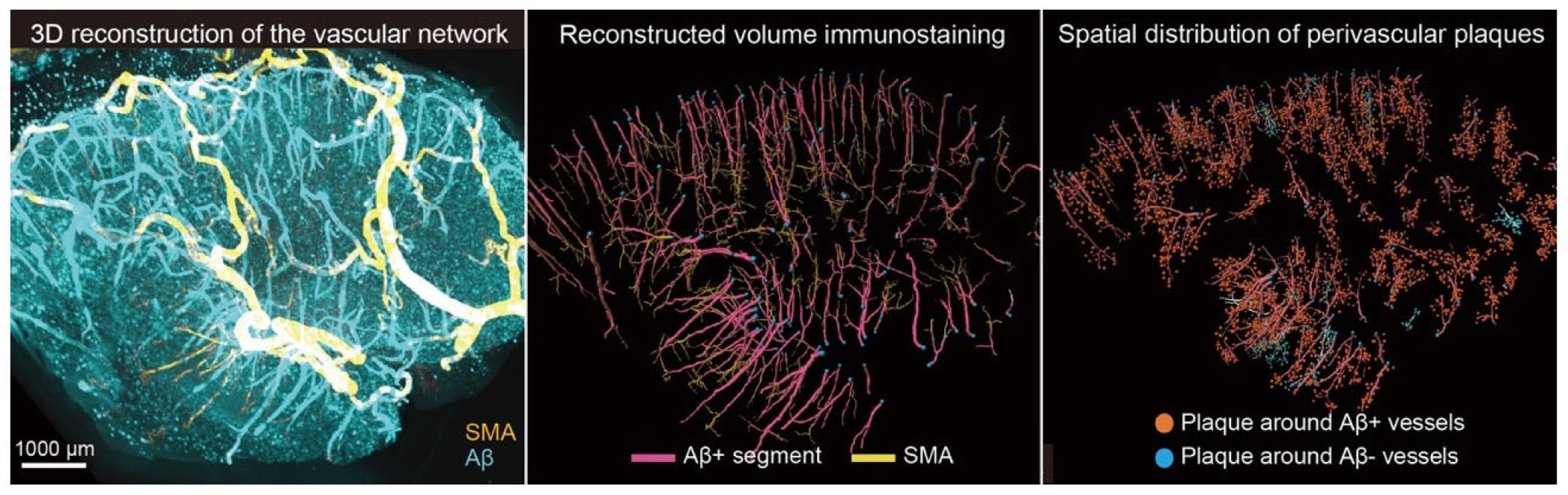
- 組織透明化と光シート顕微鏡を用いた3D解析により、ひとの脳で血管網全体とAβ沈着、老人斑の空間分布を包括的に可視化した。
- Aβ沈着は脳表動脈で最も高頻度にみられ、深部血管のみで孤立して生じることは稀であった。
- Aβ沈着血管の周囲では老人斑が少なく、血管Aβ沈着と実質Aβ沈着が相互に排他的な分布を示す可能性が示された。
- CAAおよびアルツハイマー病関連血管病変の病態理解を前進させ、脳表血管を標的とした新たな治療戦略の開発につながる。
Ⅰ.研究の背景
CAAは、脳血管壁にAβが沈着する疾患で、アルツハイマー病と高頻度に併存し、高齢者の脳出血や認知機能障害の主要な原因の一つです。これまでの研究から、Aβは脳内で産生された後に血管周囲の排出経路を通じて除去されると考えられていますが、この排出機構※1が破綻すると血管壁にAβが蓄積し、CAAを引き起こすと推測されています。Aβが血管ネットワークに沿ってどのように進展するのかについて知見は少なく、従来の二次元病理解析では、血管構造全体を立体的に捉えることが困難であり、新たな解析手法が求められていました。
Ⅱ.研究の概要・成果
本研究では、CAA患者6例の剖検脳を対象に、組織透明化技術と光シート顕微鏡を組み合わせた三次元(3D)イメージング解析※2をひとの脳へ応用しました。血管平滑筋アクチンとAβを蛍光標識し、脳表から白質に至る血管ネットワークを三次元的に解析しました。
その結果、Aβ沈着は脳表血管から深部へ連続的に進展し、深部血管のみに限局する例は極めて少ないことが明らかになりました。さらに、Aβ沈着血管の周囲では老人斑密度が低いことが示され、血管型と実質型Aβ沈着の関係を三次元的に捉えた重要な知見が得られました。
Ⅲ.今後の展開
本研究は、CAAの初期病変が脳表血管に存在し、実質内の血管分枝に連続的に広がる可能性を示すものであり、血管型Aβ沈着を標的とした新たな診断・治療戦略の基盤となることが期待されます。
Ⅳ.研究成果の公表
本研究成果は、2026年2月7日(日本時間)、米国科学雑誌 「Science Advances」のオンライン版に公開されました。
| 論文タイトル |
Expansive spatial pattern of Aβ deposition in patients with cerebral amyloid angiopathy: a three-dimensional surface-to-depth analysis (脳アミロイド血管症患者脳におけるAβ沈着の広範な空間パターンを解明:三次元でみる脳表層から深部への解析) |
| 著者 | Hideki Hayashi, Rie Saito*, Akinori Miyashita, Takeshi Ikeuchi, Mari Tada, Kohei Akazawa, Osamu Onodera, Kazuki Tainaka, Akiyoshi Kakita (*責任著者) |
| doi | 10.1126/sciadv.aea7539 |
▶ プレスリリース
Ⅴ.謝辞
本研究は、椿神経疾患研究基金、JSPS科学研究費助成事業(18H02105, 18K19373, 20K16595, 20K21246, 23H00434, 24K10617, 25K19018)、日本医療研究開発機構(AMED)(JP21zf0127004, JP24wm0625117, JP24dk0207060)などの支援を受けて行われました。
用語解説
- (※1)アミロイドβ(Aβ)は神経細胞の活動に伴って日常的に産生され、通常は脳の外へ排出されます。その主要な排出経路として、血管周囲排出経路(IPAD:intra-mural periarterial drainage)とグリンパティック経路が提唱されています。
IPADは、脳動脈の壁に沿った微細な通路を通じて老廃物を排出する仕組みで、加齢や疾患により機能が低下するとAβが血管壁に蓄積しやすくなると考えられています(1)。一方、グリンパティック経路は、脳脊髄液が血管周囲から脳実質内を循環し、老廃物を回収する排出機構です(2)。これらの機能低下は、アルツハイマー病や脳血管疾患の発症と深く関係すると考えられています。 - (※2)組織透明化技術と光シート顕微鏡を用いた三次元(3D)イメージング解析
組織透明化技術と光シート顕微鏡を組み合わせた3Dイメージング解析は、田井中教授らの研究グループが開発した、組織を薄切せずに内部構造を立体的に観察する手法です。光の散乱を抑えて組織を透明化し、シート状の光で撮影することで、大きな組織を高精細に三次元再構成できます。これにより、ヒト脳における血管構造や病変の分布を、全体像を保ったまま細胞レベルで解析することが可能になります。
参照
(1) Engelhardt B, Vajkoczy P, Weller RO. The movers and shapers in immune privilege of the CNS. Nat Immunol. 18(2):123-131 (2017).
(2) Nedergaard M. Neuroscience. Garbage truck of the brain. Science. 28;340(6140):1529-30 (2013).





