血漿p-tau217は脳アミロイド蓄積に対して脳脊髄液バイオマーカーと同等の検出精度を示す-多施設共同前向き臨床試験で実証-
2026年03月27日
概要
新潟大学医歯学総合病院 石黒 敬信 講師、同大学脳研究所 池内 健 教授らの研究グループは、東京都健康長寿医療センター、東京科学大学、九段坂病院、東京医科大学、昭和医科大学、国立病院機構西新潟中央病院、国立精神・神経医療研究センター神経研究所、東京大学、富士レビオ株式会社との多施設共同前向き共同研究を実施し、アルツハイマー病(AD)に対する血液バイオマーカー注1p-tau217(血漿注2中217位リン酸化タウ蛋白注3)が、すでに臨床応用されている脳脊髄液バイオマーカーと同等の精度で脳内アミロイドβ(Aβ)を検出できることを明らかにしました。従来、脳内アミロイドの検出には脳脊髄液検査やPET検査が行われていましたが、低侵襲性、簡便性、コスト、アクセスの面で利点がある血液バイオマーカーが臨床導入されることで、効率的かつ精度の高いAD診断が実装されることが期待されます。
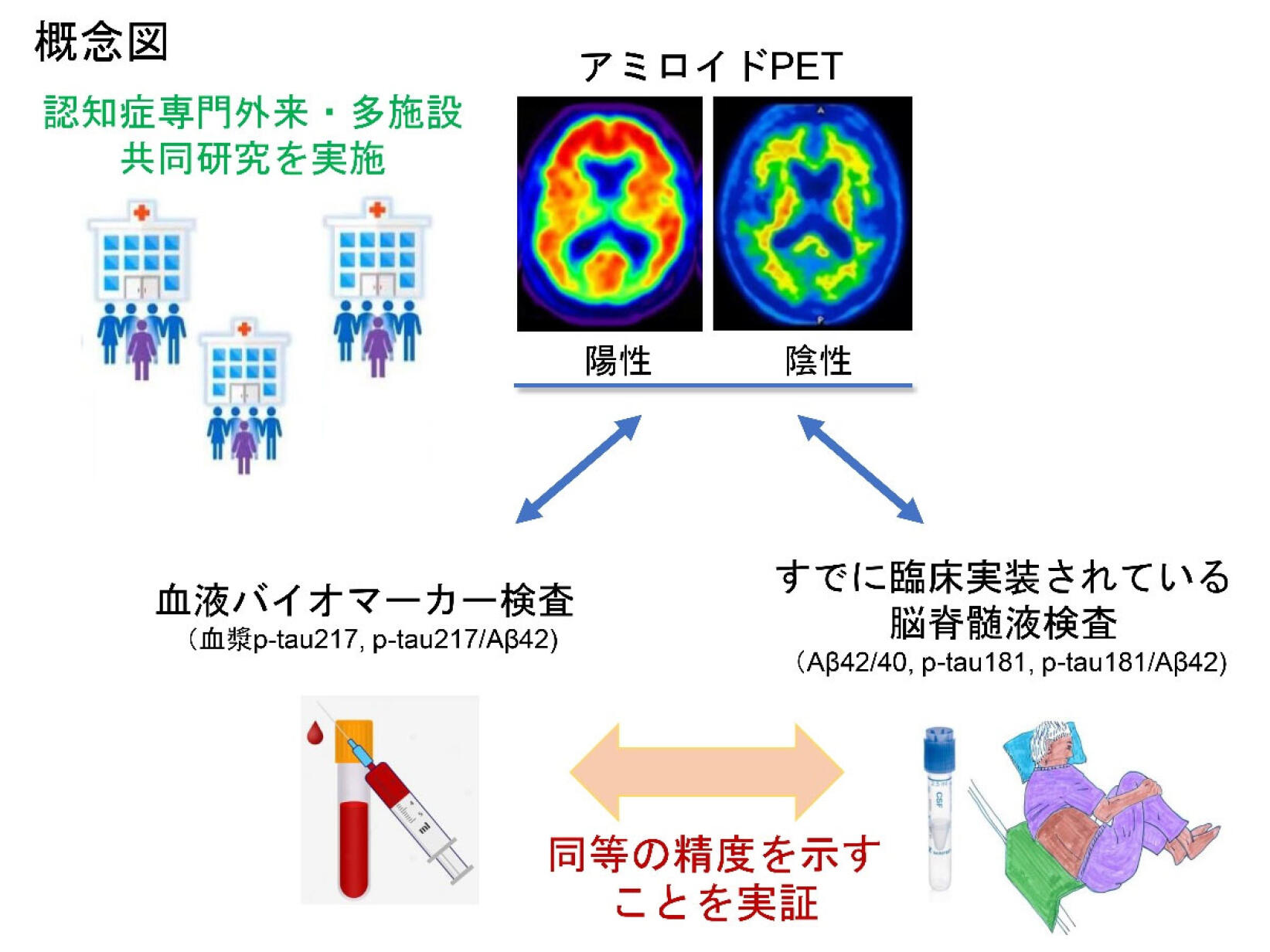
本研究成果のポイント
- 認知症専門外来を中心とした多施設共同臨床研究を実施し、血漿p-tau217とアミロイドβ 42測定の有用性を示しました。
- 血漿中p-tau217およびp-tau217/Aβ42は、すでに臨床応用されている脳脊髄液バイオマーカーと同等の精度で脳アミロイド病理を検出しました。
- 血液バイオマーカーを導入することで、約40%の被検者が脳アミロイド蓄積の可能性が低いと判断され、PET検査もしくは脳脊髄液検査の実施数を軽減できる可能性が示されました。
- 血漿p-tau217をAD診断プロセスに導入することにより、認知症に対する次世代診断フローの創出につながるものと期待されます。
Ⅰ.研究の背景
ADは認知症の中で最も頻度が高い病型であり、記銘力低下を中核に様々な認知機能障害が緩徐に進行する疾患です。臨床症状のみからADを正確に診断するのは容易ではなく、バイオマーカー検査を導入することにより診断精度が向上することが明らかにされています。分子標的治療である抗Aβ抗体薬を使用する前には、脳アミロイド病理を確認する必要があり、そのための検査として脳脊髄液検査もしくはアミロイドPET検査が保険診療により実施されています。血液バイオマーカー検査は低侵襲性、簡便性、コスト、アクセスの面で従来の検査と比較して優位性があり、認知症の次世代型診断ツールとして期待されています。血漿p-tau217を正確に測定する高感度イムノアッセイ法が開発され、血漿p-tau217が脳アミロイドを検出する有力な血液バイオマーカーとして注目されています。しかしながら、実臨床下(リアルワールド)における血漿p-tau217の有用性に関するデータは限定的でした。今回の研究では認知症専門外来を中心とした多施設共同前向き研究を行い、 血漿p-tau217を含む血液バイオマーカーの臨床有用性を検討しました。
Ⅱ.研究の概要・成果
認知機能正常者、軽度認知障害(MCI)、ADによる認知症(ADD)、AD以外の認知症(non-ADD)からなる332人の方の血漿検体を用い、p-tau217をルミパルス免疫測定法により測定しました。また、血液中のAβ42の測定を行い、p-tau217/Aβ42比を算出しました。
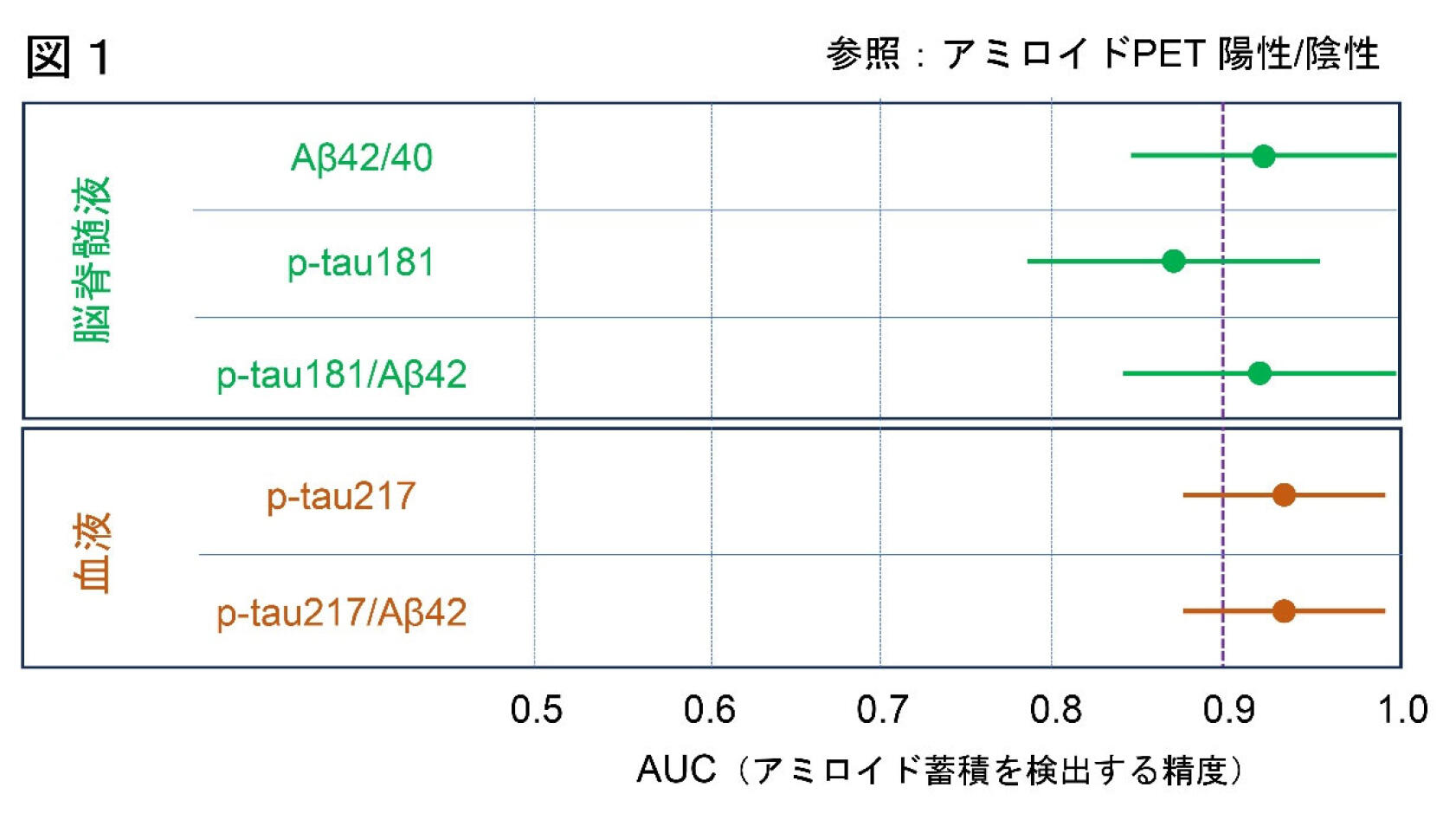
その結果、血漿中p-tau217およびp-tau217/Aβ42は認知機能正常者、non-ADD、MCI、ADDの順に高値を示しました。各カテゴリーの中では、脳アミロイド陽性者の血漿中p-tau217およびp-tau217/Aβ42は陰性者と比較して有意に高値を示しました。アミロイドPETで可視化される脳アミロイドを検出する精度は血漿p-tau217(AUC注4 = 0.93)、p-tau217/Aβ42(AUC = 0.93)と非常に高く、すでに臨床応用されている脳脊髄液バイオマーカー(Aβ42/40: AUC = 0.93, p-tau181: AUC = 0.86, p-tau181/Aβ42: AUC = 0.91)と同等の精度を示しました(図1)。
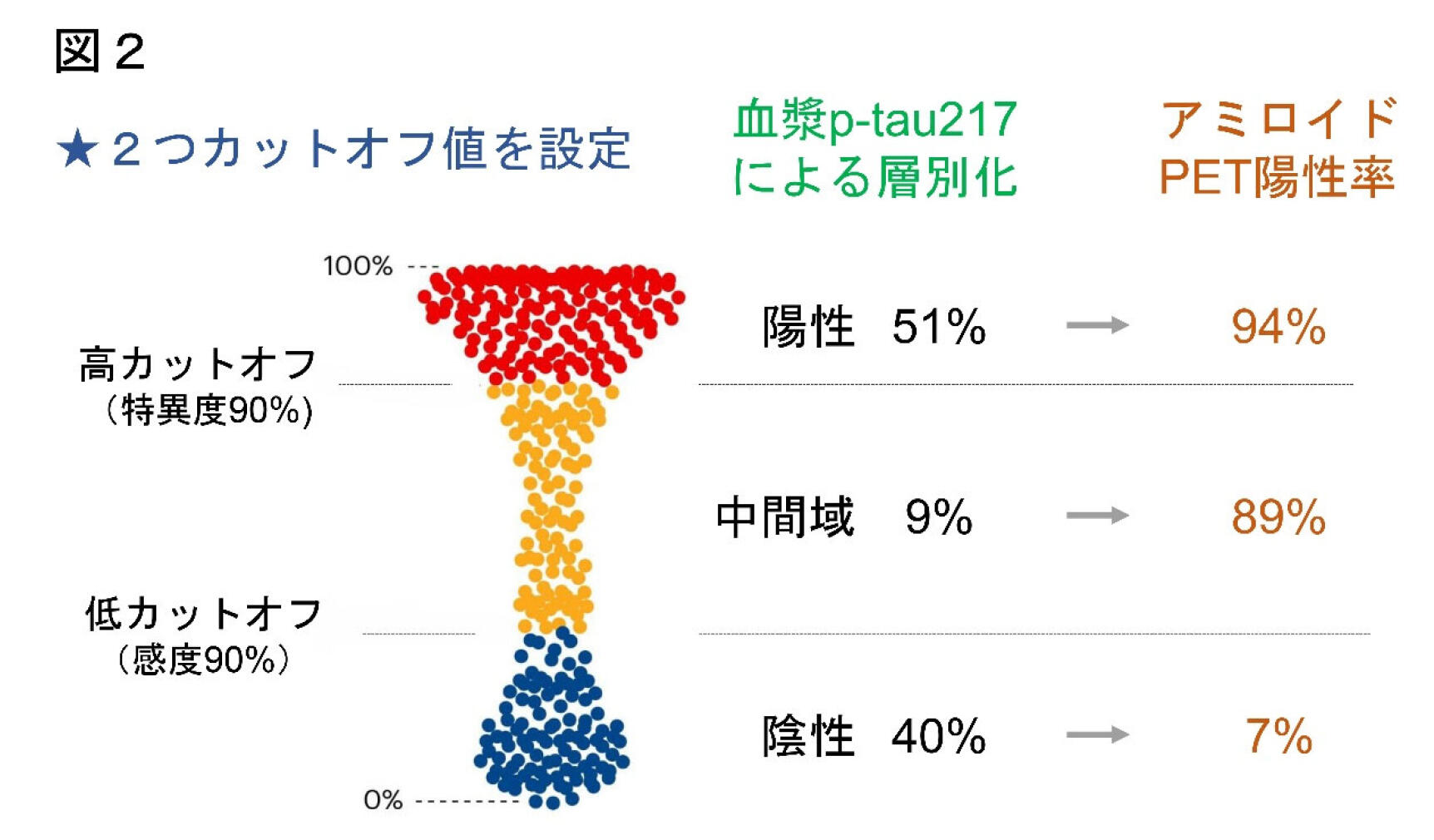
感度・特異度90%を満たす2つカットオフ値注5(高カットオフ 0.247 pg/mL、低カットオフ 0.134 pg/mL)を設定したところ、血漿p-tau217の測定値は51%が陽性、9%が中間域、40%が陰性と判定されました(図2)。血漿p-tau217の結果が陰性と判断された方のアミロイドPET陽性率は7%と低く、アミロイドを除外するためのスクリーニング検査として血漿p-tau217測定が有用であることが示唆されました。
以上のことから、血液バイオマーカーp-tau217は実臨床下において脳アミロイド蓄積を推定可能なバイオマーカーとして有用であることが示唆されました。
Ⅲ.今後の展開
今回の多施設共同前向き臨床研究により、実臨床における血漿p-tau217測定の有用性が示唆されました。今後は、血漿p-tau217測定の目的と意義を適切に設定し、臨床応用へと進めることが必要と思われます。また、血液バイオマーカー検査の事前説明、結果開示、開示後のフォローアップについての指針を臨床家の中で共有することが臨床実装に向けた課題と思われます。
Ⅳ.研究成果の公表
本研究成果は、2026年3月3日に医学誌「Alzheimer's Research & Therapy」にオンライン掲載されました。
| 論文タイトル | Prospective study on clinical utility of plasma p-Tau217 and other biomarkers in Japanese memory clinics using the LUMIPULSE platform |
| 著者 | Takanobu Ishiguro, Masanori Kurihara, Yoichiro Nishida, Emiko Kikkawa-Saito, Kensaku Kasuga, Naoto Takenoshita, Satomi Kubota, Yasuko Kuroha, Kenji Ishii, Meiko Hamada, Nobuo Sanjo, Kinya Ishikawa, Hisashi Nojima, Jo Kamada, Katsumi Aoyagi, Soichiro Shimizu, Hidetomo Murakami, Tetsuya Takahashi, Osamu Onodera, Takeshi Iwatsubo, Masahito Yamada, Takanori Yokota, Atsushi Iwata, Takeshi Ikeuchi |
| doi | 10.1186/s13195-026-01997-7 |
▶ プレスリリース
Ⅴ.謝辞
本研究は富士レビオ株式会社からの共同研究費および日本医療研究開発機構(AMED)認知症研究開発事業JP25dk0207070、東京都健康長寿医療センター 認知症未来社会創造センター(IRIDE)の助成金を受けて実施されました。
用語解説
- (注1)バイオマーカー:脳内病変や病態を反映する生物学的変化を客観的、定量的に把握するために生物学的な情報を数値化した指標を指す。
- (注2)血漿:抗凝固剤を加えて遠心分離することで得られる血液成分。血液の約55%を占める液体成分で、主に水とタンパク質で構成される。
- (注3)リン酸化タウ蛋白:AD脳に蓄積する原因蛋白。タウ蛋白が凝集しリン酸化されることで、AD脳に特徴的な神経原線維変化が形成される。
- (注4)AUC (area under the curve):ROC曲線下の面積のことで、検査の性能を表す指標。0.5から1の値をとり、1に近いほど陽性と陰性の識別能(精度)が高く、0.9以上は非常に優秀と評価される。
- (注5)カットオフ:検査結果の「陽性(異常)」と「陰性(正常)」を分ける境界となる数値のこと。感度(疾患があるもののうち検査陽性の割合)と特異度(疾患がないもののうち検査陰性の割合)がそれぞれ最適になるように、カットオフ値を設定する。





