遺伝子を改変させずにTARDBP mRNA発現の増加を誘導するモデルを報告しました
2019年07月22日
概要
新潟大学脳研究所神経内科の須貝章弘助教、小野寺理教授らの研究グループは、筋萎縮性側索硬化症(ALS)の原因遺伝子であるTARDBPの発現増加を、遺伝子を改変させずに誘導するモデルを開発しました。
運動ニューロンの損失を引き起こす致命的な神経変性疾患であるALSでは、核タンパク質であるTDP-43が、運動ニューロンの核から消失し、断片化し、細胞質中に封入体を形成します。当研究グループではこれまでに、TDP-43をコードするTARDBP mRNAがALS患者の運動ニューロンで増加していることを示していました(Koyama et al. Nucleic Acids Res. 2016)。しかし、このTARDBP mRNAの発現増加がALSの病態形成に一次的に関与しているのかどうかは、明らかではありませんでした。須貝助教らは、TDP-43動態を模したin silico modelをもとに、TDP-43病理を伴いTARDBP mRNAの増加をきたす要因のひとつには、TDP-43発現量の自己調節機構の乱れがあることを推測していました(Sugai et al. Front. Neurosci. 2018)。
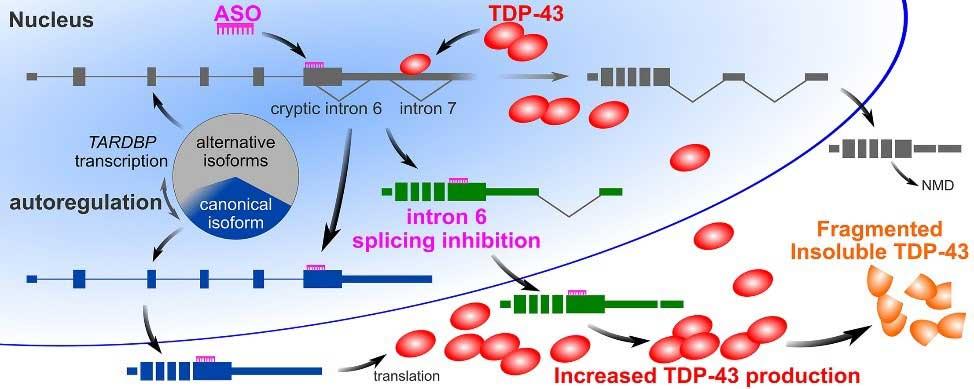
今回、研究チームは、TDP-43自己調節に重要な機構のひとつであるTARDBP mRNA選択的イントロン6のスプライシングを、アンチセンスオリゴヌクレオチドを用いて阻害しました。その結果、マウス脊髄において、TARDBP mRNA発現が2倍になり、断片化された不溶性TDP-43が増加し、運動ニューロンの数の減少がみられました。ヒトiPS細胞由来ニューロンにおいては、選択的イントロン6のスプライシング阻害はTARDBP mRNAを増加させ、核TDP-43を減少させました。 このような遺伝子を改変させずにTARDBP mRNA発現の増加を誘導するモデルの分析結果から、TDP-43自己調節の乱れがALSの病因に関連している可能性が示唆されました。本成果は、2019年7月13日に「Neurobiology of Disease」に掲載されました。
■論文はこちら