(2022年11月1日公開)
担当:石原 智彦 先生
所属:脳神経内科学分野
はじめに
<2022 ノーベル医学生理学賞>

図1 Svante Pääbo 氏
(Wikipedia より)
秋のニュースの定番の一つはノーベル賞の受賞予測です。今年は地元新聞で、本県御出身の先生の筋萎縮性側索硬化症(ALS)研究に可能性が、という記事もありまして、そうなったら私も一緒に写っている写真を使わせて頂いて、この原稿を書こうと画策しておりました。
さて、2022年10月3日にノーベル医学生理学賞の発表があり、本年度はスウェーデン人遺伝学者 スヴァンテ・ペーボ (Svante Pääbo)先生(図1)が受賞されました。いわゆるネアンデルタール人(Homo neanderthalensis)や、化石を求める人類:デニソワ人(Denisova hominin:正式な種名は未確立)のゲノム解析を行い、さらにこれらの絶滅人類と現生人類との交雑を解析された研究者になります。
当初の当ては外れましたが、この領域も個人的には興味がある分野で、何冊か一般書も読んでいましたので(広い宇宙に地球人しか見当たらない75の理由、stephen webb、青土社 などがお勧め)、なんとかこのテーマで原稿を書き上げたいと思います。
アフリカ系以外の現生人類の遺伝子には、ネアンデルタール人由来のものが数%程度含まれることがわかっています。さらにメラネシア系や、いわゆるアボリジニの方々の遺伝子には、デニソワ人の遺伝子が5%程度は含まれているようです。これらのことから、我々現生人類、ホモ・サピエンスの進化史において、絶滅人類との複数回の遺伝的交雑があったことが示されます。おそらく、未発見の古代人類との交雑もあるのでしょう。彼らから我々にもたらされた遺伝子のうち、少なくともいくつかは生存に有利に働き、現在まで保持されているものと考えらえます。
1.我々の遺伝子に残るあれこれ
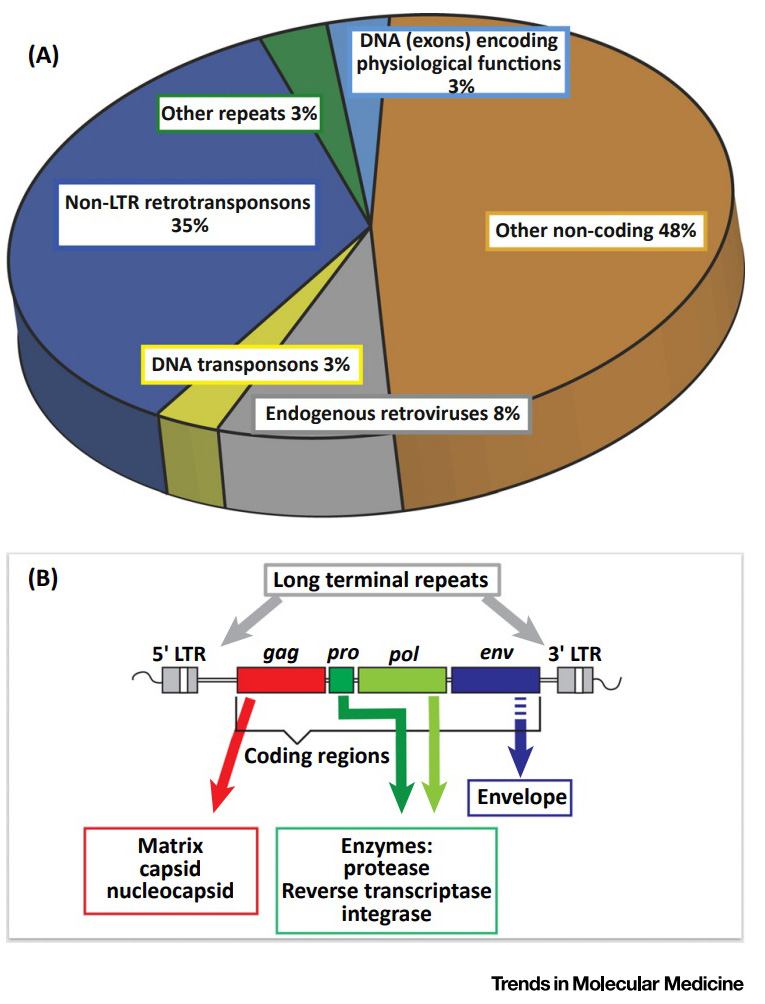
図2_文献 1)より引用
我々の遺伝子の中には、さらによくわからないものも多く潜んでいます。そもそも生理機能を有する蛋白質を発現するDNA配列部分は遺伝子全体の数%程度です。そしてヒト族から遠く離れた由来を持つ、意外な配列も我々の遺伝子の大きな部分を占めています。それは内在性レトロウイルス(ERV:Endogenous retrovirus)といわれる配列で、ヒトでは遺伝子の5-8%ほどを占めると推定されています1)(ヒト内在性レトロウイルス:HERV:Human-ERV)(図2A)。レトロウイルスというのは、逆転写酵素を持つRNAウイルスの総称です。有名なところでは後天性ヒト免疫不全症候群(AIDS)の原因となる、HIVウイルスなどがこの仲間です。gag(構造蛋白)、pol(逆転写酵素)、env(エンベロープ蛋白)といったコードを有しています(図2B)。レトロウイルスは宿主細胞に感染すると自らのRNA配列から逆転写酵素を用いてDNAを合成し、宿主細胞中のDNAに組み込まれ、自らのコピーを産生します。ERVはこのレトロウイルスのゲノムが生殖細胞に感染することにより、次世代に引き継がれていったものが由来と考えられています。幸い、現存する通常のレトロウイルスは個体に感染しても、生殖細胞には感染しません。また多くのERV、HERVは数百万年の長い年月の間に、その配列に多数の変異や欠損を生じており、ウイルスとしての活性は失っています1)。ではただのジャンクな配列かというとそういうわけでもなく、トランスポゾンと呼ばれる遺伝要素として、遺伝子発現や、発現調節に重要な役割を果たしていることが知られています。
2.HERV-K
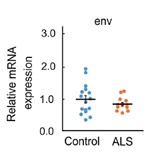
図3_文献 7)より引用
しかしERVのうち、最近組み込まれたものの一部は、機能可能なgag,pol,env蛋白を発現させることができ、レトロウイルスとしての活性を残しています。例えばコアラレトロウイルスKoRVはコアラの悪性腫瘍の原因となるウイルスですが、これは、過去数百年以内に一部のコアラにおいて内在化し、現在進行形で外来性と内在性の要素を移行しつつ、宿主であるコアラとせめぎあいながら定常状態へ向かっていると考えられる興味深いウイルスです2)。
ヒトにおいてはここまで新しい内在化レトロウイルスは知られておらず、HERVの病原性についてもまだ不明な点が多いです。しかし一部のHERVはウイルス活性を保っていることが知られており、その代表的なものにヒト内在性レトロウイルス-K(HERV-K)と呼ばれる一群があります。HERV-Kについては、神経難病の筋萎縮性側索硬化症(ALS:Amyotrophic lateral sclerosis)との関連が、Nath A.らによって報告されています1)。AIDS合併ALS症例において、抗レトロウイルス薬投与により運動神経症状が改善した報告3)や動物実験でのHERV-K env蛋白の神経毒性の証明4)、さらにはALS患者さん神経組織でのHERV-K発現増加の報告4)、等です。しかしながら、患者さん組織におけるHERV-Kの増加については、これを否定する報告も複数なされ5, 6)、意見の一致を見ていませんでした。
そこで我々は、本学脳研究所病理学分野の保有するALS患者さん15名の病理組織を用いて、脊髄および大脳運動野におけるHERV-Kの発現を測定しました7)。凍結保存された病理組織よりRNAを回収し、逆転写により相補的DNA(cDNA)を作成し、これをdroplet digital PCR法(RT-ddPCR法)で定量しました。いずれの工程も本研究所内の研究試薬、機材を用いて実施しています。組織ごとにgag,pol,envのmRNA発現量はよく相関しており、定量が正確に行われていることが示されました。しかし、正常対照群とALS患者群とで明らかな発現量の差は認められませんでした7)(図3)。今回の結果ではALSとHERV-Kの関連は否定的でしたが、抗レトロウイルス薬の臨床応用の可能性を考えると、さらなる調査が必要な領域です。
おわりに
われわれ人類の祖先をどこまでさかのぼれるかについては、ちょっと前まではカンブリア紀のピカイアと言われたり、最近はハイコウイクチスだったり様々です。ただ、人類に至る道は決して一本道でなく、様々な分岐、迂回、合流があったことが、遺伝子を調べるとわかってくるわけです。遺伝子の中の異邦人を探しながら、進化の歴史から疾患病態機序まで考えていけるのは、日々、興味深いことです。
脳神経内科 石原 智彦
参考文献
1) Kury P, Nath A, Creange A, et al. Human Endogenous Retroviruses in Neurological Diseases. Trends in molecular medicine. 2018;24(4):379-394.
2) Tarlinton RE, Meers J, Young PR. Retroviral invasion of the koala genome. Nature. 2006;442(7098):79-81.
3) Bowen LN, Tyagi R, Li W, et al. HIV-associated motor neuron disease: HERV-K activation and response to antiretroviral therapy. Neurology. 2016;87(17):1756-1762.
4) Li W, Lee MH, Henderson L, et al. Human endogenous retrovirus-K contributes to motor neuron disease. Sci Transl Med. 2015;7(307):307ra153.
5) Mayer J, Harz C, Sanchez L, et al. Transcriptional profiling of HERV-K(HML-2) in amyotrophic lateral sclerosis and potential implications for expression of HML-2 proteins. Molecular neurodegeneration. 2018;13(1):39.
6) Garson JA, Usher L, Al-Chalabi A, et al. Quantitative analysis of human endogenous retrovirus-K transcripts in postmortem premotor cortex fails to confirm elevated expression of HERV-K RNA in amyotrophic lateral sclerosis. Acta neuropathologica communications. 2019;7(1):45
7) Ishihara T, Koyama A, Hatano Y, et al. Endogenous human retrovirus-K is not increased in the affected tissues of Japanese ALS patients. Neurosci Res. 2022.






